Автор фото: Дмитрий Закревский
Последнее столетие низкотемпературной плазмой занимались для различных технологических приложений, таких как обработка поверхностей, очистка газов, создание полупроводниковых структур. В 1990-е годы задумались о практическом применении плазмы в медицине: эксперименты показали широкие возможности метода. Так, стерилизация ультрафиолетом не захватывает скрытые полости и капилляры с малым диаметром. А низкотемпературная плазма создает прямо в воздухе возбужденные молекулы, которые диффундируют в самые микроскопические полости, примерно так, как вода протекает в любое отверстие. Благодаря новому способу стерилизации многие одноразовые медицинские инструменты удалось сделать многоразовыми. Но настоящий бум интереса к холодной плазме случился в 2011 году, когда физик Майкл Кейдар из Университета Джорджа Вашингтона и его коллеги опубликовали в British Journal of Cancer статью о перспективах применения холодной плазменной струи в терапии рака.
– В 2018 году мы встречались с коллективом М.Кейдара на международной конференции, - вспоминает доктор физико-математических наук Ирина Швейгерт из Института теоретической и прикладной механики Сибирского отделения Российской академии наук. - И столь обсуждаемая тема, как терапия рака, конечно, не могла остаться незамеченной, тем более что я знала: в институтах СО РАН ведутся эксперименты с низкотемпературной плазмой. Вернувшись в Академгородок, Ирина Вячеславовна организовала коллектив и сплотила вокруг перспективной идеи сотрудников трех институтов СО РАН - родного ИТПМ, Института физики полупроводников (ИФП СО РАН) и Института химической биологии и фундаментальной медицины. Первый источник холодной плазмы сделали в ИФП СО РАН, в лаборатории Дмитрия Закревского буквально на коленке, без дополнительного финансирования, и группа Ольги Коваль (ИХБФМ) провела на клетках рака пилотные эксперименты, показавшие эффективность холодной плазмы. Но тут новосибирским энтузиастам пришел на помощь Российский научный фонд, поддержав в 2019 году проект 19-19-00255 «Низкотемпературная плазменная струя для разработки подходов противоопухолевой терапии». В 2022-м проект был продлен еще на два года. И за этот период физикам и биологам удалось продемонстрировать убедительные и вдохновляющие результаты.
– За последние 15 лет в использовании холодной плазмы достигнут впечатляющий прогресс: от стерилизации поверхностей и ускоренного заживления открытых ран у животных до клинических испытаний в онкологии, - подчеркивает руководитель проекта РНФ И. Швейгерт. - Применение холодной плазмы в противораковой терапии настолько эффективно, особенно в комбинации с химиотерапией и хирургическим вмешательством, что, возможно, мы находимся на рубеже раздела медицины на эру «до» и «после» холодной плазмы, как при открытии антибиотиков в начале прошлого столетия.
Автор фото: Дмитрий Закревский
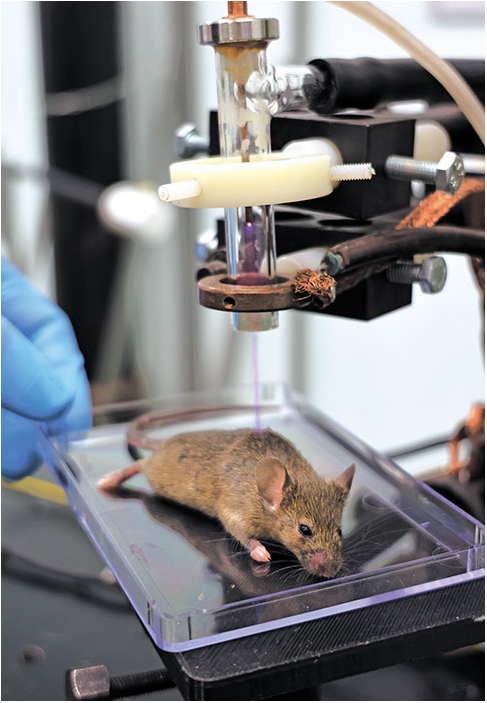
– Наше электрофизическое устройство генерирует плазму электронов и ионов, аналогичную той, что действует в газоразрядных лампах искусственного освещения. При подаче напряжения холодная плазменная струя распространяется в окружающем воздухе на 2-7 см. Высокоэнергетические электроны образуют активные формы кислорода и азота, при этом температура зоны контакта плазмы с биологической тканью не превышает 42 градусов. Наша плазма низкотемпературная, в отличие от равновесной плазмы, которая, например, есть на Солнце или в термоядерном реакторе. Энергия тяжелых частиц низкотемпературной плазмы такова, что ими можно воздействовать на биологические объекты, не вызывая их чрезмерного нагрева и, следовательно, гибели здоровых клеток. Но в новый метод надо было поверить, потому что, когда мы подавали заявку на грант РНФ, были только предварительные результаты и оригинальные идеи, требующие доказательной базы. И Фонд нас поддержал, за что ему особая благодарность, - поясняет заведующий лабораторией Института физики полупроводников им. А.В. Ржанова СО РАН доктор физико-математических наук Дмитрий Закревский.
В ходе реализации первого проекта РНФ (2019-2021) последовал настоящий шквал публикаций в высокорейтинговых журналах и докладов на российских и международных конференциях.
– Эффективность воздействия холодной плазмой напрямую зависит от правильного выбора рабочих характеристик электрофизического устройства, ее генерирующего, - комментирует И.Швейгерт. - Холодная плазма оказалась очень интересным физическим объектом. Режимы применения мы исследуем на специальной диэлектрической пластине, имитирующей кожу мыши, даже лабораторных животных стараемся лишний раз не мучить. С физической точки зрения зависимость абсолютно нелинейная. Вы вкладываете энергию, повышаете напряжение, эффект есть, потом почему-то исчезает. Воздействие вновь начинается лишь с повышением температуры, чего допустить никак нельзя. С гордостью скажу: после серьезных теоретических расчетов нам удалось с этим разобраться и выйти на нужные режимы.
Мягкое воздействие
Запатентованный сибиряками плазменный источник по виду напоминает шариковую ручку, куда вместо чернил подается благородный газ гелий. Активные радикалы (кислородсодержащие и азотсодержащие частицы) проникают в раковую клетку вместе с терапевтическими молекулами и вводят ее в мягкий апоптоз. Дело в том, что массовая гибель опухолевых клеток влечет за собой мощную интоксикацию организма, что угрожает ему смертью. А мягкий апоптоз - регулируемый процесс программируемой клеточной гибели, приводящий к плавному ее распаду.
– Уникальная особенность холодной плазмы - селективность воздействия, при которой раковые клетки убиваются, а здоровые не повреждаются, - поясняет доктор биологических наук О. Коваль из Института химической биологии и фундаментальной медицины СО РАН. - На основе анализа транскриптома раковых и здоровых клеток одного гистологического происхождения после обработки холодной плазмой получены результаты, проясняющие природу селективности. Она объясняется свойствами метаболизма раковых клеток.
На сентябрьской научной конференции 2024 года по плазменной медицине (ICPM), прошедшей в Словении, было продемонстрировано удивительное разнообразие применений газоразрядной плазмы: при лечении хронических диабетических ран, антибиотико-резистивных пленок на слизистой полости рта, для стерилизации поверхности имплантов и при пародонтозе, для коагуляции и стерилизации послеоперационных ран. Доказано, что 60-секундное воздействие плазмой временно повышает проницаемость кожи для терапевтических и косметических препаратов.
– Наш коллектив представил на этой конференции результаты исследований по комбинированному воздействию на раковые образования холодной плазменной струи с оптимизированными характеристиками и золотых наночастиц, с помощью которых увеличен вес, а, следовательно, и время жизни в опухолевой клетке терапевтических молекул, - добавляет И.Швейгерт.
Немного золота в холодной струе
Идея комбинировать воздействие холодной плазмы с проникающими в клетку наночастицами золота, к которым присоединены терапевтические молекулы, пришла в голову исследователям в 2022-м. И коллектив под руководством И.Швейгерт получил второй грант РНФ 22-49-08003 «Комбинирование воздействия холодной атмосферной плазменной струи и наночастиц для повышения эффективности плазменной противоопухолевой терапии». Было доказано, что использование золотых наночастиц усиливает цитотоксический эффект и холодная плазменная гелиевая струя в сочетании с «нагруженными» противораковыми препаратами частицами благородного металла эффективно подавляет рост опухоли in vivo.
– Применяя плазменную струю вместе с золотыми наночастицами, мы создаем в опухолевой клетке активную химическую среду для дополнительного воздействия. В статьях, опубликованных в журналах Plasma Physics Reports, Journal of Physics D: Applied Physics в конце 2024 года и Plasma Medicine в 2025-м, мы продемонстрировали, что обработка просто холодной плазменной струей приводит к значительному уменьшению опухоли, а в сочетании с золотыми наночастицами - к ее стагнации, - комментирует руководитель проекта И.Швейгерт. - Я с полным основанием утверждаю, что у нас - единственный в России междисциплинарный коллектив, значительно продвинувшийся в медицинском применении холодной плазмы. И теоретически, и экспериментально. Работа для нашей страны абсолютно пионерская, и то, что РНФ нам поверил и помог оснаститься современным оборудованием (масс-спектрометрами, установками для измерения температур, другими необходимыми приборами), дало возможность провести эксперименты по подбору режимов, цитотоксичных для злокачественных образований, но благоприятных для организма.
Разработаны способ и устройство для противораковой терапии с использованием низкотемпературной плазмы. Неинвазивный, нетоксичный метод выборочного действия. Стоит добавить, что недавно американское агентство FDA разрешило использование холодной плазмы вместо стандартного облучения для обработки околоопухолевой поверхности после операций по удалению новообразования у пациенток с раком молочной железы. Потому что низкотемпературная плазма убивает только остаточные раковые клетки, действуя гораздо гуманнее по отношению к здоровым, чем стандартная лучевая терапия.
Однако если набрать в поисковике «холодная плазма», выпадет масса предложений, прежде всего в области косметологии, за которыми не стоит ни патентов, ни теоретических обоснований эффективных режимов воздействия.
К испытаниям готовы
– Вообще-то, бездумное применение источников холодной плазмы достаточно опасно, - предостерегает О.Коваль. - Некоторые режимы воздействия могут вызвать не апоптоз, а пролиферацию (разрастание ткани путем размножения делением) раковых клеток. Мы это видели в экспериментах.
Эффективность воздействия на опухолевые образования определяется выбором режима генерации плазменной струи. Необходимо не только создать коктейль активных радикалов в окружающем воздухе, но и увеличить проницаемость мембраны раковых клеток. Малые дозы воздействия холодной плазмой способствуют заживлению ран, но неприменимы в противораковой терапии. Наш плазменный источник с 2019 года прошел ряд модификаций и тестов на животных.
Сотрудники ИФП СО РАН и ИТПМ СО РАН оптимизировали рабочие режимы электрофизического устройства, а верификация их эффективности проводилась на клеточных моделях и животных со специально привитыми опухолями сотрудниками ИХБФМ СО РАН. Были найдены оптимальные рабочие амплитуды, частоты и формы импульсов напряжения, смеси газов и время воздействия холодной плазменной струи. Изучение характеристик плазменного источника проводилось на основе анализа токов у поверхности объекта облучения, спектров химического состава, температуры в зоне воздействия и, конечно, выживаемости раковых клеток после обработки. Для эффективной борьбы с разными типами раковых клеток (а мы проверили более 10 видов рака) требуются индивидуальные режимы обработки холодной плазменной струей.
Разработанные нами прибор и метод не уступают зарубежным аналогам и готовы к доклиническим, а затем и клиническим испытаниям, но нужны партнеры из практической медицины, поддержка на государственном уровне и, конечно, средства.
Эксперименты в Германии продемонстрировали настоящие чудеса: если привить подопытной мыши две опухоли, а плазмой воздействовать только на одну из них, вторая тоже гибнет, поскольку активная химическая среда стимулирует мощный иммунный ответ организма. Согласитесь, такой подход очень эффективен в случае наличия метастазов. Исследования показали: механизмами воздействия холодной плазменной струи на раковые клетки являются окислительные процессы, запускаемые активными формами кислорода и азота, которые плазма генерирует в окружающем воздухе, и умеренные электрические поля, увеличивающие проницаемость мембраны клеток.
Анализ экспрессии протеинов продемонстрировал разнонаправленные изменения в здоровых и раковых клетках.
Портативный источник холодной плазмы может открыть замечательные перспективы для российских клиник. Один из основных его плюсов - умеренная цена и удобство в использовании. К тому же онкологией сфера применения холодной плазмы отнюдь не исчерпывается. Другие перспективные направления - обработка ран в нестерильных условиях, лечение грибковой инфекции, герпеса, псориаза, иных кожных заболеваний. И, наконец, уже упомянутая косметология.
Более того, удручает российская и мировая статистика по удалению диабетической стопы: две трети случаев гнойно-некротического процесса заканчиваются ампутацией конечности. Между тем обработка холодной плазмой позволяет такие раны излечивать.
Ольга КОЛЕСОВА












![[Центр коллективного пользования]](/img/logo-ckp.gif)
![[Контакты]](/img/contacts.gif)
![[Служба webmail]](/img/webmail_new.gif)
![[Библиотека]](/img/lib_new.jpg)
![[Закупки]](/img/gos.gif)